수산화 마그네슘

| |
| |
| 이름 | |
|---|---|
| IUPAC 이름
Magnesium hydroxide
| |
| 별칭
Magnesium dihydroxide
Milk of magnesia | |
| 식별자 | |
3D 모델 (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.013.792 |
| EC 번호 |
|
| E 번호 | E528 (산도 조절제, ...) |
| 485572 | |
PubChem CID
|
|
| RTECS 번호 |
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| 성질 | |
| Mg(OH)2 | |
| 몰 질량 | 58.3197 g/mol |
| 겉보기 | White solid |
| 냄새 | Odorless |
| 밀도 | 2.3446 g/cm3 |
| 녹는점 | 350 °C (662 °F; 623 K) decomposes |
| |
용해도곱 (Ksp)
|
5.61×10−12 |
자화율 (χ)
|
−22.1·10−6 cm3/mol |
굴절률 (nD)
|
1.559[1] |
| 구조 | |
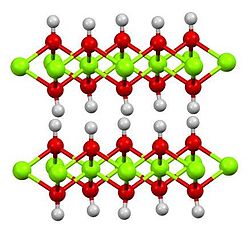
| Hexagonal, hP3[2] | |
| P3m1 No. 164 | |
a = 0.312 nm, c = 0.473 nm
| |
| 열화학 | |
열용량 (C)
|
77.03 J/mol·K |
표준 몰 엔트로피 (S
|
64 J·mol−1·K−1[3] |
표준 생성 엔탈피 (ΔfH⦵298)
|
−924.7 kJ·mol−1[3] |
기브스 자유 에너지 (ΔfG˚)
|
−833.7 kJ/mol |
| 약리학 | |
| A02AA04 (WHO) G04BX01 | |
| 위험 | |
| 물질 안전 보건 자료 | External MSDS |
| GHS 그림문자 |  [4] [4]
|
| 신호어 | 경고[4] |
| H315, H319, H335[4] | |
| P261, P280, P305+351+338, P304+340, P405, P501[4] | |
| NFPA 704 (파이어 다이아몬드) | |
| 인화점 | Non-flammable |
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |
LD50 (median dose)
|
8500 mg/kg (rat, oral) |
| 관련 화합물 | |
다른 음이온
|
Magnesium oxide |
다른 양이온
|
|
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
수산화 마그네슘(Magnesium hydroxide)은 약염기 이온결합 물질이다. 수산화 마그네슘은 물에 대한 용해도가 매우 낮아 물에 혼합하게 되면 용액이 과포화되어 우유와 흡사하게 하얀빛을 띈다. 이 때문에 '마그네시아의 우유'라는 별칭이 있다. 주로 제산제의 주성분으로 사용하며, 엽산과 철, 칼륨 흡수를 방해한다. 수산화 마그네슘 암석은 수활석이라고 한다.[5]
제법
[편집]마그네슘 염에 수산화 알칼리를 작용시켜 콜로이드 형태로 침전되는 수산화 마그네슘을 얻는다.
- Mg2+ (aq) + 2 OH− (aq) → Mg(OH)2 (s)
공업적으로는 수활석에서 채취하거나 해수로부터 반응시켜 대량으로 생산한다.
용도
[편집]의학적 용도
[편집]수산화 마그네슘 현탁액은 주로 제산제나 설사약으로 사용된다. 또, 칼륨 흡수를 억제하기 때문에 고칼륨증 치료에도 사용하나 그 외 용도에 사용할 때 부작용으로 저칼륨증과 근육통을 야기할 수 있다. .[6] 또한, 겨드랑이 냄새 탈취제로도 사용하며,[7] 국소적 구내염 및 구강 궤양에 사용하기도 한다.[8] 과다 복용시 고 마그네슘증의 위험이 있다.
산업적 용도
[편집]수산화 마그네슘은 인체에 무해하기 때문에 산성 폐수를 중화하는데 사용한다. 또한, 수산화 칼슘과 함께 산호를 이루는 주성분이기에 인공 산호를 제조하는데 사용된다. 그리고 흡열 분해점이 332 ° C로 높기 때문에 다른 물질, 반응에 첨가시 발화점을 높히고 연기가 적게 나게 한다.
- Mg(OH)2 (s) → MgO (s) + H2O (g)
또한, 연소시 산소를 흡수하고 물을 생성하여 가연성 물질을 제거하기 때문에 화재 방지용으로 플라스틱 제품, 지붕등에 코팅하기도 한다.[9][10][11][12]
신진 대사
[편집]수산화 마그네슘은 복용양에 따라 사용 목적이 나뉜다.
성인 복용 기준으로 0.5g ~ 1.5g의 수산화 마그네슘을 복용하게 되면, 다음과 같은 반응이 일어나 위액 속 염산을 중화시킨다.
- Mg(OH)2 (s) + 2HCl (aq)→ MgCl2 (aq) + 2H2O (l)
이 보다 많은 2g ~ 5g을 섭취 할 경우, 중화 되고 남은 다량의 수산화 마그네슘이 주변 소화관에 흡수되어 농도를 높히고, 삼투압 현상으로 인해 소화관이 주변 세포조직으로부터 물을 흡수하게끔 만든다. 그 결과, 연동운동이 활발해지며 대변을 부드럽게 한다. 남은 수산화 마그네슘은 소장에 일부 흡수된다. 이 과정에서 신부전증을 앓고 있는 환자는 혈변 증상을 일으킬 수도 있다.
각주
[편집]- ↑ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ↑ Toshiaki Enoki and Ikuji Tsujikawa (1975). “Magnetic Behaviours of a Random Magnet, NipMg(1-p)(OH2)”. 《J. Phys. Soc. Jpn.》 39 (2): 317–323. doi:10.1143/JPSJ.39.317.
- ↑ 가 나 Zumdahl, Steven S. (2009). 《Chemical Principles 6th Ed.》. Houghton Mifflin Company. A22쪽. ISBN 978-0-618-94690-7.
- ↑ 가 나 다 라 “Magnesium Hydroxide”. American Elements. 2019년 5월 9일에 확인함.
- ↑ “Magnesium Hydroxide”. University of Michigan. 2007년 1월 9일. 2011년 1월 16일에 원본 문서에서 보존된 문서. 2015년 1월 10일에 확인함.
- ↑ Magnesium Hydroxide – Revolution Health
- ↑ “Milk of Magnesia Makes Good Antiperspirant”. 2007년 4월 2일에 원본 문서에서 보존된 문서. 2015년 1월 10일에 확인함.
- ↑ Canker sores, 2/1/2009
- ↑ Hollingbery, LA; Hull TR (2010). “The Fire Retardant Behaviour of Huntite and Hydromagnesite - A Review”. 《Polymer Degradation and Stability》 95 (12): 2213–2225. doi:10.1016/j.polymdegradstab.2010.08.019.
- ↑ Hollingbery, LA; Hull TR (2012). “The Fire Retardant Effects of Huntite in Natural Mixtures with Hydromagnesite”. 《Polymer Degradation and Stability》 97 (4): 504–512. doi:10.1016/j.polymdegradstab.2012.01.024.
- ↑ Hollingbery, LA; Hull TR (2012). “The Thermal Decomposition of Natural Mixtures of Huntite and Hydromagnesite”. 《Thermochimica Acta》 528: 45–52. doi:10.1016/j.tca.2011.11.002.
- ↑ Hull, TR; Witkowski A; Hollingbery LA (2011). “Fire Retardant Action of Mineral Fillers”. 《Polymer Degradation and Stability》 96 (8): 1462–1469. doi:10.1016/j.polymdegradstab.2011.05.006.
외부 링크
[편집] 위키미디어 공용에 수산화 마그네슘 관련 미디어 분류가 있습니다.
위키미디어 공용에 수산화 마그네슘 관련 미디어 분류가 있습니다.
| 이 글은 화학에 관한 토막글입니다. 여러분의 지식으로 알차게 문서를 완성해 갑시다. |

